NEWS CENTER
新闻中心
干细胞临床试验汇总
关于“渐冻症”——间充质干细胞、神经干细胞和诱导多能干细胞的疗效比较
2024-12-31
浏览次数:
一、引言
ALS 是一种进行性神经退行性疾病,主要特征为脊髓、脑干和运动皮层的运动神经元死亡,导致肌肉逐渐萎缩、痉挛、瘫痪,最终死亡。其确切病因尚不清楚,约 90% 为散发性,10% 为家族性。目前治疗主要针对炎症、兴奋性毒性、易聚集蛋白和蛋白病等分子机制,但效果有限。干细胞疗法作为一种多靶点治疗方法,正受到广泛关注。
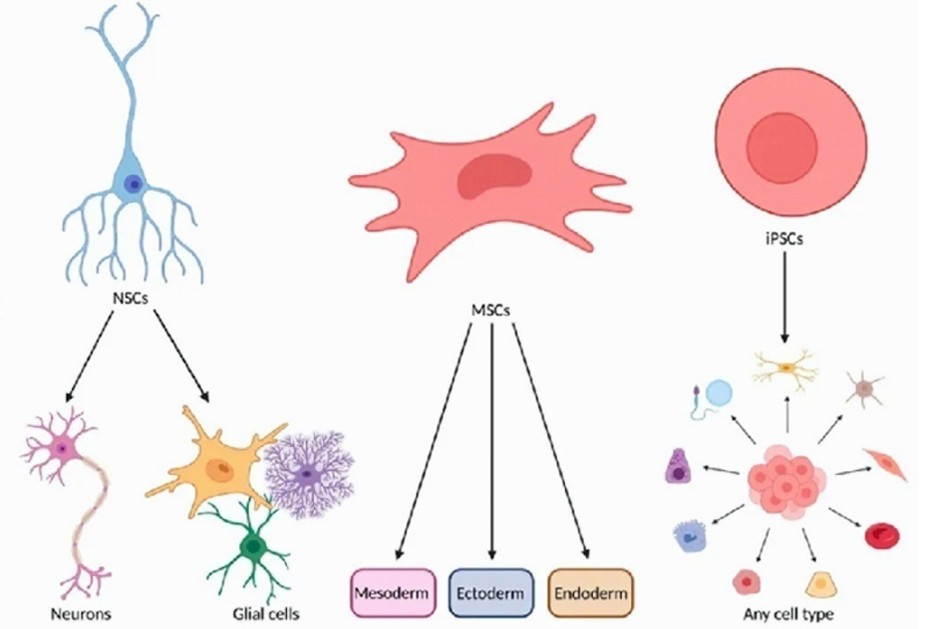

二、间充质干细胞(MSCs)在 ALS 治疗中的应用
来源与特性
MSCs 可来源于骨髓、脂肪组织和脐带血等,具有自我更新、多向分化和免疫调节能力,能分泌多种生长因子和细胞因子,发挥神经保护和再生作用。 临床研究
Siwek 等人的研究发现,鞘内注射自体骨髓间充质干细胞(BMD-MSCs)在部分晚期症状患者中可减缓疾病进展,但在进展较慢的患者中效果不明显。该研究存在非随机、无对照和样本量小的问题。 Terashima 等人的实验研究表明,骨髓来源的单核细胞与表达生长因子的 MSCs 联合应用,可改善 ALS 小鼠模型的运动功能、延长生存期并减少神经胶质增生,但研究存在样本量小、治疗效果不一致等局限。 一项回顾性研究显示,鞘内注射自体 BMD-MSCs(lenzumestrocel)可能提高长期生存率,但回顾性研究的可靠性需进一步验证。 脂肪组织来源的间充质干细胞(ASCs)通过其分泌组发挥治疗作用,包括生长因子、细胞因子和外泌体等,可调节基因表达、促进血管生成和神经元修复。在转基因小鼠模型实验中,ASCs 来源的外泌体可增强运动功能、保护神经元,但动物模型研究存在伦理问题,需临床验证。 脐带间充质干细胞(UC-MSCs)方面,UC-MSC 衍生的条件培养基(UCMSC-CM)可延长 ALS 模型小鼠寿命、减轻神经炎症,但动物模型结果外推至人类存在局限,且缺乏对照。Wang 等人对 UC-MSCs 衍生的运动神经元进行基因修饰,在小鼠模型中观察到运动性能改善和生存期延长,但研究存在局限性。目前有多项临床试验正在评估 MSCs 在 ALS 治疗中的安全性和有效性,如 ALSUMMIT 试验等,但结果尚未公布或存在一定局限性。
三、神经干细胞(NSCs)在 ALS 治疗中的应用
来源与特性
NSCs 是多能干细胞,可从胎儿脊髓或大脑中分离,能分化为神经元、星形胶质细胞和少突胶质细胞。 临床研究
多项动物模型试验表明,将人 NSCs(hNSCs)注射到 SOD1G93A 啮齿动物模型中,在疾病早期有一定益处,但存在细胞迁移有限、分化不完全、对晚期疾病改善作用小等问题,且研究存在遗传背景变异和结果不一致等情况。 早期人体试验主要关注 hNSC 鞘内注射的安全性和耐受性,已进行的两项 I 期临床试验和一项 II 期临床试验显示,该方法相对安全,部分患者有短暂功能改善,但由于样本量小、疾病进展快、缺乏疗效评估设计等原因,无法得出明确结论。Cedars - Sinai 医学中心的试验使用基因修饰的祖细胞(CNS10 - NPC - GDNF)治疗 ALS,初步结果显示安全性良好,但长期效果和样本量问题仍需进一步研究。
四、诱导多能干细胞(iPSCs)在 ALS 治疗中的应用
来源与特性
iPSCs 由患者特异性体细胞重编程而来,具有无限自我更新和分化为所有细胞类型的能力,可绕过胚胎干细胞的伦理问题,实现个性化治疗。 临床研究
多项研究表明,iPSCs 在动物模型中显示出治疗潜力,如改善运动功能、保护运动神经元和减少神经胶质激活等。Yang 等人开发了将 iPSCs 定向分化为颈脊髓运动神经元的方法,Marshall 等人发现 iPSC 衍生的运动神经元在特定突变情况下有轴突再生增强的潜力。 然而,iPSC 治疗面临一些问题,如基因毒性和表观遗传异常风险,虽总体安全性较好,但仍需关注。其生成和分化技术复杂,成本高昂,限制了临床应用。目前多数研究为临床前试验,人类研究数据有限,需要更多随机对照试验来评估其安全性和有效性。
五、干细胞疗法的未来方向
间充质干细胞(MSCs)
尽管 MSCs 在临床试验中显示出一定疗效,但存在 MSC 特性变异、临床结果不一致等问题。未来需要进行更多 III 期和 IV 期临床试验,规范研究设计和细胞制备方法,比较不同来源 MSCs 的疗效,开展联合治疗和生物标志物分析,以确定最佳治疗方案。 神经干细胞(NSCs)
NSCs 在动物模型和早期人体试验中表现出一定潜力,但面临伦理问题、侵入性操作、细胞迁移和存活有限以及疗效不确定等挑战。未来应改进细胞移植技术,提高 NSC 的存活和迁移能力,开展更大规模的随机对照试验,纳入更多样化的患者群体,开发可靠的生物标志物来监测治疗效果,同时结合其他治疗方法和基因编辑技术,以提高治疗效果。 诱导多能干细胞(iPSCs)
iPSCs 具有个性化治疗的潜力,但在生成、分化和应用过程中存在技术复杂性、成本高、肿瘤发生风险和基因组不稳定性等问题。未来需要优化 iPSC 的生成和分化方法,降低成本,加强质量控制,评估潜在风险,开展更多临床研究,建立综合数据库以深入了解 ALS 机制,推动 iPSCs 在临床治疗中的应用。 联合治疗
干细胞联合治疗是一种有前景的方法,在其他神经退行性疾病中已显示出一定优势,但在 ALS 中的研究较少。未来需要进一步研究其在 ALS 治疗中的应用,评估不同细胞组合的协同效应和安全性,以确定最佳联合治疗方案。
六、结论
干细胞疗法为 ALS 治疗带来了新的希望,MSCs、NSCs 和 iPSCs 各有其独特的治疗潜力和局限性。未来需要进一步深入研究和开展大规模临床试验,以优化干细胞治疗方案,提高治疗效果,改善 ALS 患者的预后。
参考文献:




