新闻中心
干细胞临床试验汇总
7名患者连续5天雾化吸入干细胞外泌体!结果显示干细胞外泌体可修复病毒感染后导致的损伤
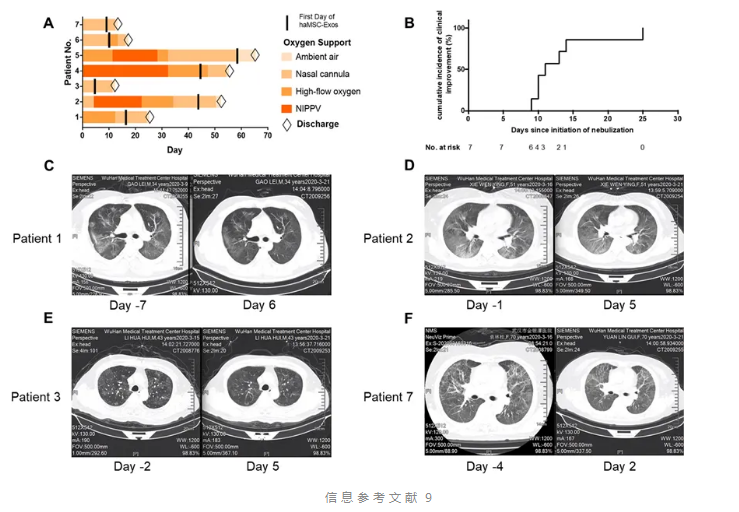
最近,甲流进入高发期。甲流传播途径主要是通过呼吸道飞沫,病毒侵入人体后迅速复制,导致细胞损伤和炎症反应。临床数据显示,雾化吸入干细胞外泌体能够迅速被肺部细胞吸收,从而快速发挥其抗炎和修复作用。文献案例表明,7名新冠病毒感染患者在接受日剂量为2.0 × 10^8 纳米囊泡(间充质干细胞外泌体)后,所有患者肺部病变均有不同程度的消退,7例患者中有4例消退较明显。这些临床数据表明,间充质干细胞外泌体雾化有潜力成为养肺护肺的新选择。
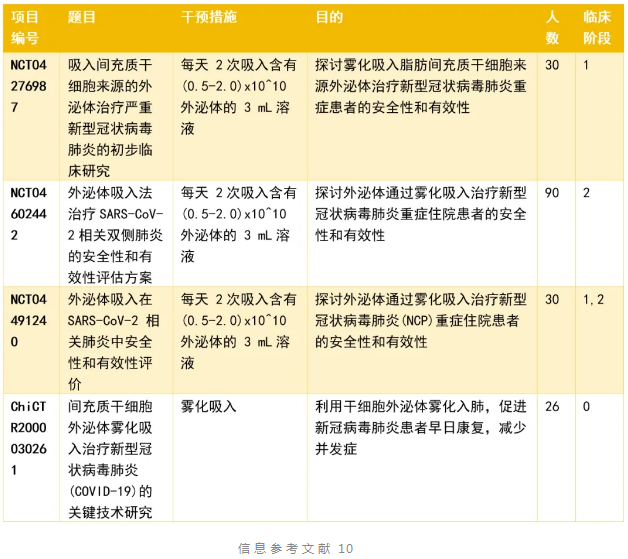
雾化吸入干细胞外泌体,可修复肺部炎症及损伤
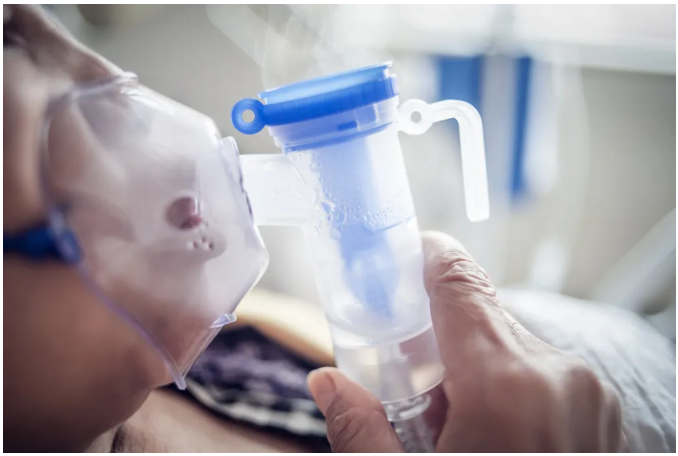
雾化吸入的干细胞外泌体能够迅速被肺部细胞吸收,从而快速发挥其抗炎和修复作用。
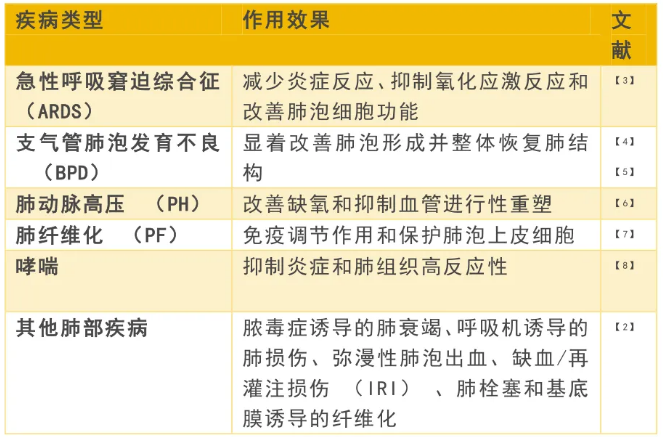
案例盘点:雾化吸入干细胞外泌体,修复病毒感染后的肺部损伤
近年来,利用干细胞外泌体雾化吸入来修复病毒感染导致肺部损伤的临床数据越来越多,也为干细胞外泌体雾化吸入护肺养肺提供了新的思路。
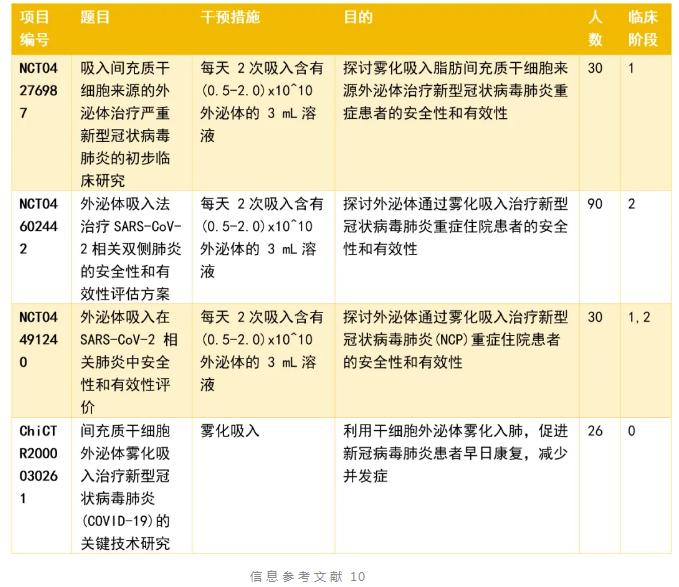
干细胞外泌体雾化的优势
靶向作用:外泌体可以被设计成靶向病毒或感染的细胞,通过携带特定的抗病毒分子或免疫调节剂,直接作用于感染部位,提高治疗效率。
免疫调节:外泌体可以携带免疫调节分子,如抗炎因子或免疫激活分子,帮助调节机体对病毒的免疫反应,减轻炎症反应,防止过度的免疫应答导致的组织损伤。
抗病毒作用:外泌体可以携带抗病毒药物或RNA干扰分子,通过雾化吸入直接到达肺部,抑制病毒复制,减少病毒负荷。
减少全身副作用:由于外泌体是通过雾化吸入直接作用于肺部,因此可以减少药物在全身的分布,降低可能的副作用。
同时,雾化吸入外泌体可以与药物相结合,在流感季节前或早期接触病毒后使用,以减少感染风险或减轻症状,更好更快恢复健康。
甲型流感是一种常见的呼吸道传染病,现有的治疗方法虽然有效,但仍有局限性。雾化吸入外泌体作为一种新兴的治疗手段,在治疗肺部疾病方面展现出巨大潜力。未来,随着外泌体的制备、优化、临床前和临床试验的进一步取得进展,这一前沿技术有望为病毒感染后的肺部修复带来革命性的进步,帮助更多的患者养肺护肺。
1. Sophia Ng,Raffael Nachbagauer,Ángel Balmaseda, et al. Novel correlates of protection against pandemic H1N1 influenza A virus infection. Nature Medicine. 2019;25 (6):962-967. doi:10.1038/s41591-019-0463-x
2. Azhdari, M.H.; Goodarzi, N.; Doroudian, M.; MacLoughlin, R. Molecular Insight into the Therapeutic Effects of Stem Cell-Derived Exosomes in Respiratory Diseases and the Potential for Pulmonary Delivery. Int. J. Mol. Sci. 2022, 23, 6273.
3. Zheng, Y.; Liu, J.; Chen, P.; Lin, L.; Luo, Y.; Ma, X.; Lin, J.; Shen, Y.; Zhang, L. Exosomal miR-22-3p from human umbilical cord blood-derived mesenchymal stem cells protects against lipopolysaccharid-induced acute lung injury. Life Sci. 2021, 269, 119004.
4. Cassady, S.J.; Lasso-Pirot, A.; Deepak, J. Phenotypes of Bronchopulmonary Dysplasia in Adults. Chest 2020, 158, 2074–2081.
5. Bancalari, E.; Jain, D. Bronchopulmonary Dysplasia: 50 Years after the Original Description. Neonatology 2019, 115, 384–391.
6. Thompson, A.A.R.; Lawrie, A. Targeting Vascular Remodeling to Treat Pulmonary Arterial Hypertension. Trends Mol. Med. 2017, 23, 31–45.
7. Zhang, E.; Geng, X.; Shan, S.; Li, P.; Li, S.; Li, W.; Yu, M.; Peng, C.; Wang, S.; Shao, H.; et al. Exosomes derived from bone marrow mesenchymal stem cells reverse epithelial-mesenchymal transition potentially via attenuating Wnt/beta-catenin signaling to alleviate silica-induced pulmonary fibrosis. Toxicol. Mech. Methods 2021, 31, 655–666.
8. Papi, A.; Brightling, C.; Pedersen, S.E.; Reddel, H.K. Asthma. Lancet 2018, 391, 783–800. ain, K.K. An Overview of Drug Delivery Systems. Methods Mol. Biol. 2020, 2059, 1–54.
9. Zhu YG, Shi MM, Monsel A, Dai CX, Dong X, Shen H, Li SK, Chang J, Xu CL, Li P, Wang J, Shen MP, Ren CJ, Chen DC, Qu JM. Nebulized exosomes derived from allogenic adipose tissue mesenchymal stromal cells in patients with severe COVID-19: a pilot study. Stem Cell Res Ther. 2022 May 26;13(1):220. doi: 10.1186/s13287-022-02900-5. PMID: 35619189; PMCID: PMC9135389.
10.张雨晴,吴军.间充质干细胞及其外泌体治疗2019冠状病毒病的机遇与挑战[J].中国组织工程研究(010):027[2025-01-21].




