新闻中心
干细胞基础知识
如何理解干细胞的归巢性才不会出错
干细胞可以自己找到自己的“家”,而这个家是指适合她自己生存的地方,就像识途老马一样,永远知道自己的家在哪里——这就是我们所说的“归巢”。干细胞可以从自己家出来在外周血中“溜达”一圈,再寻找到并进入微环境适宜的“niche”中并定居其中,安居乐业。
-01-
要想全面了解干细胞的归巢性,首先我们得知道这个词是怎么来的。
“归巢”(homing)最早是指循环在血液中的淋巴细胞倾向于迁移到它们原先派生自那里的淋巴细胞部位(如淋巴结),这一回归现象称为“淋巴细胞的归巢”,这是1983年Gallation提出来的 [1] 。后来“归巢”这一概念逐渐引申至干细胞。
干细胞归巢是指内源或外源性干细胞在多种因素的作用下,能定向趋向性迁移,越过血管内皮细胞至靶向组织并定植存活的过程,类似人体局部炎症反应后大量白细胞迁移至炎症周围。
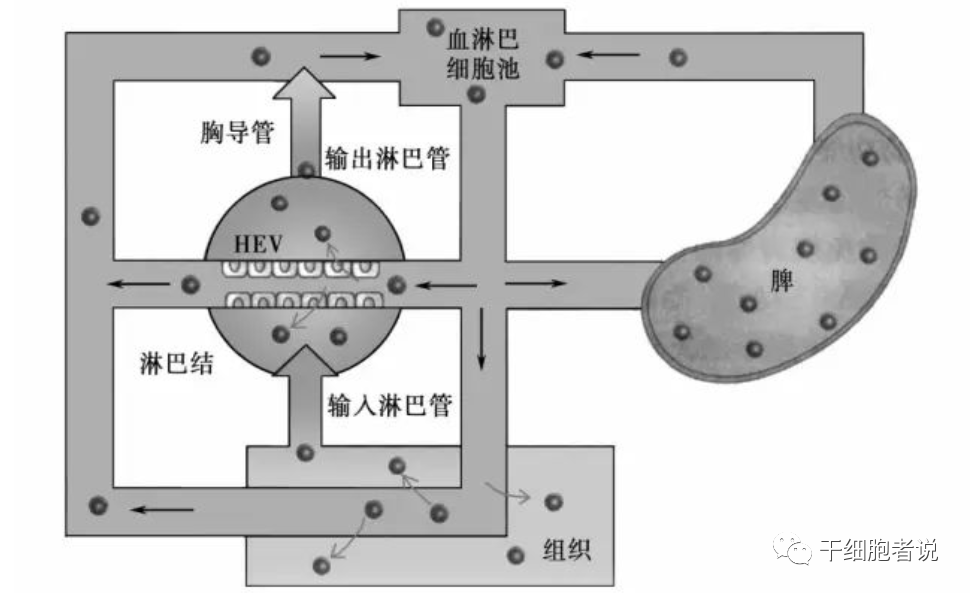
▉ 概念:干细胞巢(niche)
-02-
微环境改变是MSCs 归巢的始动因素,组织损伤局部表达多种趋化因子、黏附因子、生长因子等各种信号分子。不同的微环境(组织微环境或病理微环境)分泌不同的信号分子,吸引MSCs定向到达该组织。干细胞归巢,最终归巢至骨髓,归巢至各个脏器,归巢至炎症及创伤部位,甚至归巢至肿瘤部位。
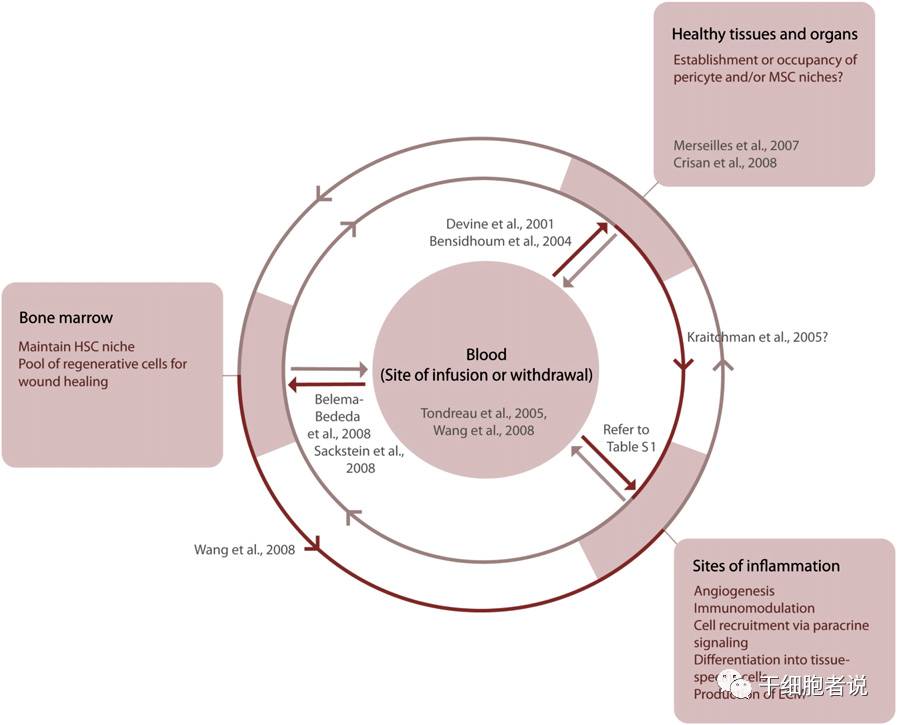
J.M.; Leng, T.G. . Cell Stem Cell 2009, 3, 206-216
图注:间充质干细胞在不同的解剖位置发挥着不同的功能。炎症反应包含创伤、慢性炎症反应(如移植物抗宿主病)和肿瘤等。[3]
一句话:干细胞归巢性,犹如一部GPS,时刻指引着干细胞寻找安“家”的路。
-03-
干细胞的归巢机制具体尚不明确。许多研究指出,MSCs 的归巢效应所涉及的物质与白细胞向炎症组织归巢的效应十分相似。简而言之,某些特定信号分子与MSCs膜上相应受体结合,共同驱动其归巢行为。移植的干细胞顺利归巢至微环境,这要求损伤部位的信号分子和MSCs表面受体相一致,这也是决定MSCs移植的成败之一。
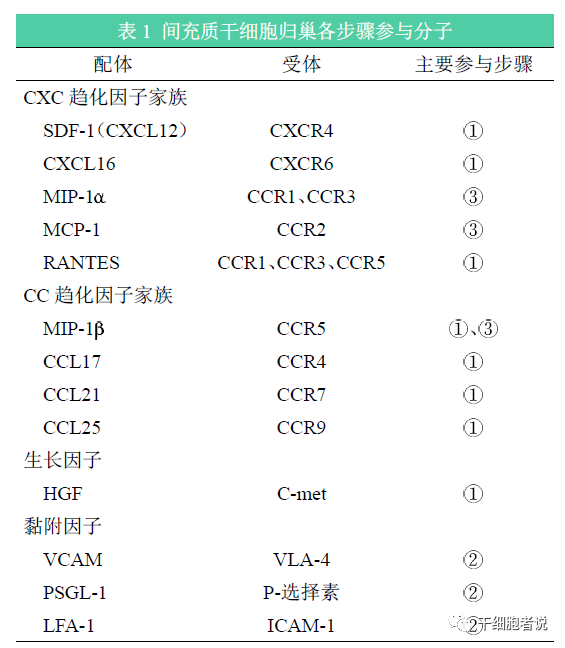
Ann De Becker 等[4]提出MSCs 在治疗各类疾病时,表现出了牢固的黏附、爬行、扩散和跨内皮细胞迁移的过程。参与归巢行为的小组成员很多,有诸如趋化因子、生长因子和黏附分子等。
特定的组织分泌特定的趋化因子,并且通过趋化因子的浓度梯度,吸引带有趋化因子受体的细胞定向到达该组织。在损伤过程中,不同组织细胞能释放不同的化学趋化因子,这些趋化因子能促进MSCs迁移。
以CXCR4受体为例,一般只与CXCL12相结合。在骨髓含有较多CXCL12趋化因子,因此骨髓中的造血干细胞中经常可以发现CXCR4受体的存在[5] 。一般而言,趋化受体能够感受外部环境趋化因子浓度,并引导细胞到达趋化因子浓度较高的地方[6] 。
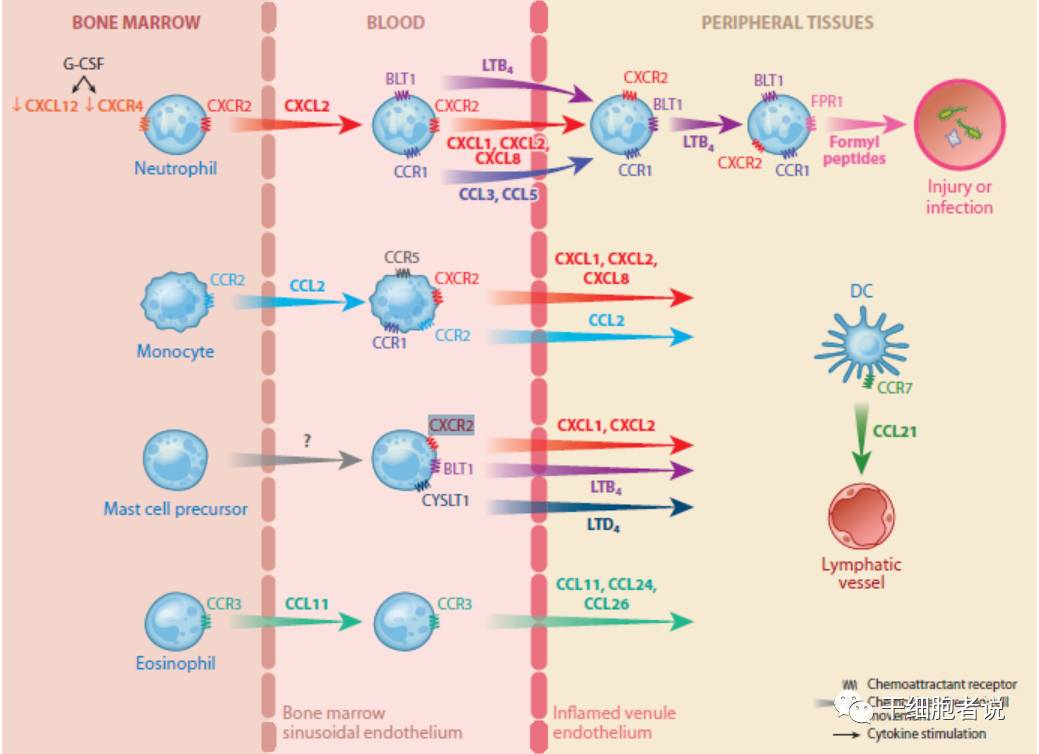
▉ 黏附分子:主要负责由外而内
血管中的MSCs黏附于毛细血管壁跨内皮细胞层归巢至目标组织,MSCs和细胞外基质通过表达细胞黏附分子配体与细胞黏附分子结合,介导干细胞归巢到特定的靶点。黏附分子是MSCs 完成归巢过程中不可缺少的成分。此外,炎症因子(如TGFα等)与生长因子(如HGF等)也是归巢小组的重要成员。
▉ 穿越内皮,各就各位
在MSCs完成归巢动员及黏附内皮后,想要发挥其治疗作用,仍需从血液循环中迁移出来,从而进入损伤部位。而穿越血管内皮细胞是其主要途径。在此过程中各种趋化因子、金属蛋白酶(MMP)和纤维连接蛋白(FN)发挥着重要作用。
Clements等[8]发现FN暴露的V区是MSCs 上VLA-4 的一个结合点,它们结合后使MSCs能够黏附到血管内皮外,从而进入细胞外基质。
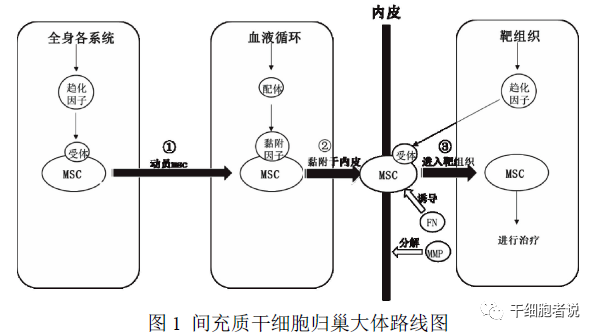
注: 间充质干细胞归巢大体路线图。
-04-
MSCs反复传代会导致其干性丢失,影响其治疗效果。MSCs在体外发生老化以及细胞间的氧化损伤积累,使细胞的增殖和归巢潜能有所减弱。
MSCs的移植方式
干细胞目前最主要的移植方式是动脉移植、静脉移植、局部注射移植。静脉回输常发生静脉停滞于肺部而影响疗效,但胜在操作简单;动脉注射操作复杂,创伤大,出血多;局部注射归巢率高,疗效好。
MSCs的黏附贴壁的处理
黏附贴壁是移植干细胞存活、生存和有效的前提。研究发现,在移植前使MSCs的处于黏附贴壁状态会有利于移植后的细胞生存和向目标组织的归巢。所以,处于培养期的MSCs效果要比刚解冻后的MSCs要好。
MSCs的移植时间、数量
移植时间及数量影响其归巢的效果,MSCs细胞越早期,移植后归巢率越高。如果数量够,不经过体外培养最好。Rombouts等 [7] 研究表明,新鲜分离的原代MSCs较培养传代后的细胞归巢能力更强。MSCs培养24 小时其归巢效率可从55%~65%降至10%,但对于刚分离出的原代MSCs往往数量稀少,通常要在体外进行大量培养扩增,以增加干细胞数量。所以,移植时间与细胞数量也是一个矛盾。




